ժҪ��ÿ��2��ע��FSH���M(j��n)��ţ�ij��ű��̎���î�(d��ng)����t���ڻ��Ӽ��g(sh��)�ˆT���`��������߳���ʧ���Ŀ�����������҂��O(sh��)Ӌ��3��ԇ��(y��ng)�����|(zh��)�����A(ch��)�ľ���SRF��ϡጴ�������V���Ȼ��δμ����(n��i)��IM��ע����ţ�����M(j��n)�г���Ч�����u�������ԇ�1������ţ�ֳ�3�M����M(j��n)��ÿ��2�ε�ע������c2�Nע�䷽���Č����о�������4�죬ÿ��2�Σ����սM����IM��ţ��n=6���ij��ŷ���(y��ng)�������چδ�Ƥ�£�ע��SC��SRF��n=6���������ţ��n=6���δ�IM��SRF�ķ���(y��ng)λ�ڃ���֮�g��ԇ�2�������^�δ�IMע������������ɷNSRF�ĝ�ȣ�20mg/ml�����|(zh��)�������100% ����10mg/ml�����|(zh��)�ᣬ50%��Ӱ������Y(ji��)���S�w��CL����ƽ����(sh��)�]���@�����P≥0.05�����������������/��̥��(sh��)��P��0.05����������ܾ��ѣ�P��0.01���Ϳ���ֲ��̥��(sh��)��P��0.001��������100% SRF̎���M��n=20���ǃ�(y��u)��50% SRF̎���M��n=20��������ԇ�3����ڼtɫ����˹��ţ�ό��Ȇδ�IM 100% SRF ϡጵ�FSHЧ����������c���y(t��ng)�Ğ���4�����ÿ��2�εij���Ч����CL��ƽ����(sh��)��13.7±1.2 VS 13.8±1.2�������������̥��(sh��)��12.3±1.5 VS 13.7±1.2������ܾ��ѣ�7.2±1.1 VS 8.4±1.4���Ϳ���ֲ��̥��4.9±0.8 VS 6.4±1.3�����ڌ��սM��n=29���͆δ�ע��M��n=29���Л]���@���������
1. ǰ��
��ţ����̎������ҪĿ�����T�l(f��)��������ѣ���ʹ�a(ch��n)������Ŀ���ֲ��̥����ֲ��ĸ��������������Ȼ����������w���ڴ����ټ��ص�̎���кܴ��׃���ԣ��䌦��̥��ֲҲ����Ҫ��Ӱ������������l(f��)�����ں����ݲ����о��M(j��n)չ�������������ݲ����ӵĕr���ü���̎�팢�@���^�õij���Ч��������ݲ���ͬ�چ��ӷ����F(xi��n)�������^��(y��u)���O(sh��)Ӌ��
���wţ�ij���̎������ͨ�^���y(t��ng)�Ćδ�IM ���RѪ������ټ��أ�eCG���������ÿ��2��IM���w��ȡ��FSH�팍�F(xi��n)�����RѪ������ټ�����һ�N��(f��)�s���ǵ������������˥�ڞ�40С�r�����δ�ע��������������FSH����ţ�w��(n��i)�������˥�ڲ���5С�r����횶��̎�������T�l(f��)��������ô��w��ȡ��ÿ��2�ε�IM̎���ij��ŷ���(y��ng)��(y��u)��ÿ��1�ε�̎����������ˣ����w�����D�ص�̎�����֔(j��n)�������t�����e�`̎��؛ע�䌢���ʧ���Ŀ����ԣ������������ÿ�Ճɴε�̎�팢�����wţ���^�ȑ�(y��ng)����������@��ʹ���Ժ�ij��ŷ���(y��ng)��u�p�����ʺ��ε����ݳ��ų���?q��)������p�ٹ��wţ�ij���̎���M�������������䷴��(y��ng)��������������䌦����̎���Ą�������������
�ô��w�����FSH-P�����������z�}��ý��ϡጺ�һ���Կ���ע����Ч�������ÿ�Ճɴ������5��ij��ų���Ȼ��������@�δ�ע��Įa(ch��n)���Ŀ���ֲ��̥��(sh��)�dz�������������Ҳ��FSH�������X���z��۾Sͪ�Ƅ����������Y(ji��)������(w��n)���������Ȼ����Ҳ��һ����(d��n)�n���Ǵ��w��ȡ����@Щ������ij����������ʹ��ţ�w��(n��i)�a(ch��n)����FSH �Ŀ��w�
�δ�ע��FSH����?q��)��ǂ��y(t��ng)��ÿ��2��̎�������ţ����̎�����x��;��֮һ��������δ�̎��������ܸ����m����ȱ�ټ��g(sh��)�ˆT��ţ���������һ�ʹ�ô��w����ȡ�������������V�����о�����������δ�Ƥ��ע��400mg NIH-FSH-P1������ţ��ý���������w�r�^�ߣ���3/5����ţ�ij��ŷ���(y��ng)�c���y(t��ng)��ÿ��2���������4���̎���Y(ji��)�����ƣ�Ȼ����������˽Y(ji��)�������^��Ƥ��֬���M���ĺ�˹̹��ţ��δ���؏�(f��)������һ헺�˹̹��ţ���о�����������δ�ע���FSH-V���ֳ�2����������̎���ĵ�һ��Ƥ��ע��75%��48С�r��ע��ʣ���25%�������ǰ������������ע������������ŷ���(y��ng)�c���y(t��ng)��4��̎������]�в�ͬ������������V�Ćδ�Ƥ��ע���cţ���w�r���������P(gu��n)������������ܳ���̎����ţ�����õ�����(y��u)��Ч���������
һ�����x�õķ�(w��n)���Ćδ�FSHע��ij��ŷ���(y��ng)��(y��ng)ԓ�nj���������V�Ϳ����オ�Y(ji��)�Ͻ�ĸ߷��Ӿۺ�����Y(ji��)��������S���ڎ����(n��i)��(w��n)�����ٵ�ጷż��ء��кÎN�����ϳɵIJ�ͬ�������|(zh��)�ľۺ�������ھS��ˎ��ľ���ጷ�������@Щ���|(zh��)�ǿɽ����������������w�M���]�����߷���(y��ng)���m�����ڄ����w��(n��i)ʹ����������һ�N���������|(zh��)�����A(ch��)�����|(zh��)��SRF���������ǰ���о��У��͌���������V��SRFϡጺ�δ�ע���M(j��n)�����w�������T�l(f��)���ŷ���(y��ng)�������һϵ�еČ���O(sh��)Ӌ-�u��ʹ��SRFϡጵĴ�������V�δ�IM������������ţ�ij��ŷ���(y��ng)����ҪĿ���Ǵ_��ʹ��SRFϡጺ�Ĵ�������V�δ�ע���λ�c���������ŷ���(y��ng)�ķ�(w��n)���ԣ�ԇ�1������������^�ɷN��ͬ��ȵ�SRF��IMע��Y(ji��)�������2����������ڰ���˹��ţ�����������^ע��SRFϡጺ��������V��ע��ÿ�Ճɴε������}ˮ���C��ǰ���T�l(f��)���ŷ���(y��ng)���������
2. �����c����
���1����SRFϡጺ�Ĵ����ݼ���Vע�䲻ͬλ�c�ı��^���s�N������ţ��n=18�����S�C�ķֳ�3�M������ڵ�0�죨�_ʼ̎���죩��������е���ţע��5mg 17β-�ƶ�����50mg�м��أ���ֲ�뺬1.56g �м��ص�ꎵ�˨������ڵ�4�����������̎���M(j��n)����ţ�ij���̎������һ�M�����սM�����������}ˮϡ�400mg�� NIH-FSH-P1�������ÿ��2���i��IMע����u�f�pע��4�죨80��80,60,60,40,40,20,20������ڶ��M����10ml��SRF��20mg/ml ���|(zh��)�ᣩϡ�400mg�� NIH-FSH-P1�i��IMע�䣻 �����M������10ml��SRFϡ�400mg�� NIH-FSH-P1����Ƥ�£�SC��ע�����������چδ�ע�䣬���Ȍ���������V��1ml�������}ˮϡ������Ȼ��ע���M(j��n)����9ml���������Ȟ�22mg/ml �����|(zh��)���Сƿ�������p�u�����������M(j��n)12ml��ע�������M(j��n)��ע������ڵ�6������Ϻ����磨FSH�_ʼ̎�����48С�r�����������ţע��150mg PGF�������������糷˨��������ڵ�8�������ע��12.5mg��LH���������12��24С�r���M(j��n)��ݔ��������������ţ�ڵ�7�����緀(w��n)�����������������12С�r���M(j��n)��LH��ע���ݔ������ڵ�15������g(sh��)���ռ���̥���������IETS�ķ����u���|(zh��)����IETS�u���|(zh��)����1��2������̥�t�J(r��n)���ǿ���ֲ����̥������
���2�DZ��^2�N��ͬSRF���ͨ�^�δ�IMע���������V���ŷ���(y��ng)������2�A���M(j��n)��̎�������һ�A�Σ�15�^�tɫ����˹��ţ�������O(sh��)Ӌ�M(j��n)�Ѓɴγ���̎��������ڶ��A���������10�^�tɫ����˹��ţ�S�C�ֳɃɽM��������M(j��n)��һ�γ���̎������ڵ�4��r�����Ռ��1�Ćδ�̎��������400mg��NIH-FSH-P1�M(j��n)���i��IMע����������δ�ע���ԇ���nj���������N�ă��ɷ�ĩ��1ml�������}ˮϡ������Ȼ����12ml��ע�������c9ml��SRF��22mg/ml ���|(zh��)�����100%��Һ������50%��SRFϡጣ�11mg/ml ���|(zh��)���������50%��Һ����̎��ǰ���ݔ������̥�ɼ����u�������Ռ��1���M(j��n)��̎��������
���3���C��ǰ��ĽY(ji��)�������������^��100%��SRFϡጵĴ�������V�Ćδ�IMע��͂��y(t��ng)�������}ˮϡጵĴ�������V��ÿ��2�ε�IMע�䌦�tɫ����˹���w��ţ�ij���Ӱ����������փɂ��A�Σ���1�A���������17�^�tɫ����˹��ţ�������O(sh��)Ӌ�M(j��n)�Ѓɴγ���̎���������ڶ��A�Σ�24�^�tɫ����˹��ţ�S�C�ֳɃɽM�������M(j��n)��һ�γ���̎�����ڵ�4��r���������Ռ��1����400mg��NIH-FSH-P1��ÿ�ՃɴΞ���4����f�p�δ��M(j��n)���i��IMע�䣬�δ�ע���ԇ���nj���������N�ă��ɷ�ĩ��1ml�������}ˮϡ�����Ȼ����12ml��ע�������c9ml��SRF��22mg/ml ���|(zh��)��������100%��Һ����̎��ǰ����������ͬ���2������ݔ�����������̥�ɼ����u�������Ռ��1���M(j��n)��̎������
2.1 ����
���е���ţ�ڵ�0��͵�4��z���S�w�Ĵ�������������ݵĴ�С�͔�(sh��)���������ţ���ѳ��ڳ���̎�����g��4-8�죩���ÿ�춼�M(j��n)���������L���Եij����z�y�������11��z�y���є�(sh��)���������15��ͨ�^ֱ�c�z���S�w��(sh��)�����C�����ŷ���(y��ng)������
2.2 �y(t��ng)Ӌ����
���1�еĔ�(sh��)��(j��)���B�m(x��)�Ġ�B(t��i)�ֲ���׃������ANOVA�M(j��n)���u���������ƽ����(sh��)ͨ�^LSD�yԇ�M(j��n)�б��^��������2��3�Ĕ�(sh��)��(j��)ͨ�^ƽ�����������D(zhu��n)����Ȼ��ʹ��Infostat�M(j��n)��ANOVA���������ͨ�^���o(h��)LSD�yԇ�M(j��n)��ƽ����(sh��)�ı��^������ANOVA���ģʽ�z�y�씵(sh��)�������̎�����씵(sh��)�c̎��������≥9mm����ֱ���͔�(sh��)����Ӱ�����̎���M�gƽ������ֱ���Ľy(t��ng)Ӌ���^���ÿ�^ţ��ƽ������ֱ�����ѳ��ϳ��F(xi��n)����3mm�����ݕr�_ʼ�M(j��n)�Мyԇ�������
3. �Y(ji��)��
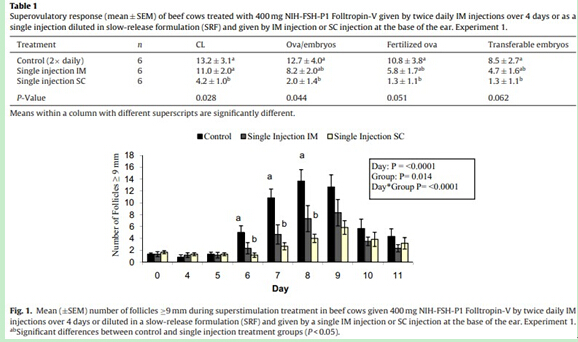
���1�ĽY(ji��)�����1��ʾ����������̥��(sh��)������ܾ��ѺͿ���ֲ��̥��(sh��)������400mg FSH��ÿ��2�Ξ���4���IMע��Ȱ�400mg FSH�δζ���SCע��Ч���@���ã�P��0.05���������Æδ�IMע���@�õĿ���̥��(sh��)��������ܾ��ѺͿ���ֲ��̥��(sh��)̎�����gˮƽ��������c����̎���M�g�]�@���������D1��ʾ���ڳ���̎�����gֱ��≥9mm��ƽ�����ݔ�(sh��)�������е�̎���M��������ֱ��≥9mm��ƽ�����ݔ�(sh��)�ڵ�5-8��r���ӣ����ڵ�һ��FSH̎�����24С�r��������˺�t�p�٣����Ӱ푣�P��0.001�������������������6-8����������ÿ��2��IMע���������V�ķ�������������и����≥9mm���������������
��ԇ�2����ڵ�1��2�A��֮�g�������]�в��������Ԍ���(sh��)��(j��)�Y(ji��)����һ�𡣱M��CL��ƽ����(sh��)�]���@���IJ�����������������/��̥��(sh��)��P��0.05��������ܾ��ѣ�P��0.01���Ϳ���ֲ��̥��(sh��)��P��0.001����100% SRF��Һ�ı�50% ��Ҫ�õĶࣨ��2������������̥�ɼ��r����50%SRF�M�е�2�^ţ��100%�е�1�^ţ�������S�w��(sh��)С��2����������������50%SRF�M��20�^ţ���8�^��ţ��40%���]�Юa(ch��n)���κο���ֲ����̥���������100%�M�е�������ţ���a(ch��n)��������һö����ֲ��̥�������
��̎�����g���ݵ����ԛ]��ʲô��ͬ������ע���������V�Į�(d��ng)��ֱ����3-5mm�����ݔ�(sh��)����4������ 18.6±1.5 VS 16.4±1.6���������є�(sh��)��13.2±1.1 VS 10.4±1.4�������LH̎�����ƽ�����ѕr�g��30.8±1.3h VS 30.1±2.6h����100%SRF ϡጽM��50%ϡጽM�M�g�]���@���������Ȼ�������������ֱ����3mm��P=0.0662�����D2����≥9mm��P=0.08994��������D3����������̎�����g���A���Еr�g��̎��֮�g�Ļ����������ʹ���ڵ�7��͵�8�죬��100% SRF ϡጵĴ������ؽM��50%�ĽM�и����ƽ������ֱ��ֵ���D2����≥9mm�����ݔ�(sh��)���D3������
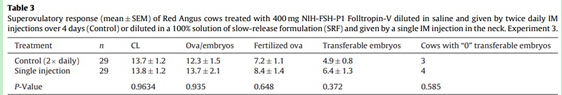
��ԇ�3������ڵ�1��2�A��֮�g���]�в���������Ԍ���(sh��)��(j��)�Y(ji��)����һ��CL�Ĕ�(sh��)�������������̥��(sh��)������ܾ��є�(sh��)�Ϳ���ֲ��̥��(sh��)�ڽM�g�]�в��P��0.05�����3�����������̥�ɼ��r�������ÿ�M����1�^ţ���S�w��(sh��)≤2������սM����1�^�͆δ�ע��M����2�^��ţ�]�a(ch��n)���κο���ֲ��̥��
��̎�����g�M�g�������ԛ]��ʲô���������ֱ��≥3mm���D2�������ݵ�ƽ��ֱ������ֱ����3-5mm������6-8mm��≥9mm�����ݔ�(sh��)���ܵ��씵(sh��)��Ӱ푣�P��0.001�������ǽM�g�]���@���IJ����Ҳ�]�л���Ӱ������������������ע���������V�Į�(d��ng)��ֱ����3-5mm�����ݔ�(sh��)����4�����19.6 ± 1.5 VS 17.6 ± 1.3)�����є�(sh��) (15.8±1.3 VS 14.5 ±1.7) LH̎�����ƽ�����ѕr�g (31.3± 2.3 h VS 35.1 ± 2.3 h)��������ڌ��սM�͆δ�ע��M֮�g�]���@������
4 ӑՓ
���ĽY(ji��)���@ʾ����20mg/ml�����|(zh��)�ᣨ100%��SRF��Һ��ϡጴ�������V����������M(j��n)�Іδ�IMע���������t����˹���wţ�и��õij���Ч�����ڮa(ch��n)������̥����(sh��)�Ϳ���ֲ��̥��(sh��)��������c���y(t��ng)��ÿ��2�ε�IMע���Ч���]���@��������ֵ��ע������ڌ��2��3�У�49�^ţ��100% SRFϡጴ�������V���M(j��n)�Іδ�ע��������H��4�^��8%���]�a(ch��n)���κο���ֲ��̥����@����ǰ��������P(gu��n)��ţ��24%���ͺ�˹̹��ţ��ÿ�Ճɴ�IMע��Ĕ�(sh��)ֵҪС�����H���������ڌ��3�У�ÿ�Ճɴ�IMע���29�^����ţ���սM��������H��3�^��10%���]�Юa(ch��n)������ֲ��̥������@Ȼ�͆δ�IMע��ij��ŷ���(y��ng)�M֮�g�]�в�������
ע���ѪҺ�е�FSH������������̎������λ�c�ʹ��x����IJ�ͬ���������մ��x���������A(y��)�yFSH����ͬ�����ʱ���������oՓ̎���ķ����͝�������������w��ȡ��Ŀ������Ռ���(d��o)������������ʼӿ��������������������^���ȵ�FSH�����L�r�g�p�٣����ܾS��������ǰ������ǰ���īI(xi��n)�Y(ji��)���@ʾ������������V�����}ˮϡ�������چδ�IM��SCע��������̈́����ѪҺ��FSH�_(d��)�����Ƶĸߝ��������������w�r�^�ý����ˆδ�SCע�����ţ�w��(n��i)��FSH�½�������������Ɯy�������w�r�õ���ţ�����^����ԭ����������FSH�þ���ϩ�ȿ���ͪϡጣ��Ȍ��յ������}ˮϡጌ���(d��o)�������ո����������r�g���L��ѪҺ��FSH��ȸ�������҂��Ɣ�����������V�����|(zh��)����Ҳ���p�������ٶȣ��S��ѪҺ��FSH���^��ˮƽ���������������چδ�ע���������V�T�l(f��)���ŷ���(y��ng)���������FSH������������Ӱ����أ���������������������
ԇ�1�ĽY(ji��)���@ʾ���������������V�����|(zh��)���φδ�SC����ע�䣬�]�Юa(ch��n)���^�õ�Ч����������δε�IMע���Ŀǰ�ѽ��ܵ�ÿ��2�ε������}ˮϡጵ�̎��Ч���]���@���IJ���M���ڔ�(sh��)ֵ��Сһ�c���������Ȼ���������������V�����|(zh��)���ϵķ�����ֵ�Å����������20mg/ml�����|(zh��)�ᣨ100% SRF����Һ�Ƿdz�ճ��������������ϴ�������V���ǿ����^��ĵ������������Բ�����Сƿ����ȫ�ij������������������Ɣ��δ�IMע����^�͵ij��ŷ���(y��ng)����������FSH��ԭӋ���Ą���С�ľ����������Փ�����ݵ���ֳ�����Ͽ��C����������M���ڼ���̎���_ʼ�r���������������ݣ�3-5mm����(sh��)���]�в�������_(d��)��9mm�����ֱ�����چδ�ע��M���^�ٵģ��D1���������ʱȴ�������V��20mg/ml�����|(zh��)���ϵķ�����������߀��̽��һ�N������ȡ�ķ������@Ҳ���҂��ڌ������ʹ���^�͝�ȣ�10mg/ml���|(zh��)���������50% SRF�������|(zh��)���ԭ��50% SRF��Һ����ʮ��ճ���ʸ�����Сƿ����ȡ���
�ڌ��2��3�У���ע������(n��i)��������}ˮ�еĴ�������V��SRF��Һ������������ŷ���(y��ng)������Ч����Ȼ�������50%��SRF��Һ��100%�ij���Ч������������ڌ��2�У����ݵ�ֱ�������@ʾ��50%��SRF�ܽ��������V���T�l(f��)���ŷ���(y��ng)�����������ݵ����L�ƺ������t2���6�죻�D2�����������100% SRF�M���D3�����F(xi��n)���^�ٵ����_(d��)�����Ѵ�С����������Ɯy�������ں�벿��̎��r��FSH�����ԭ��������ǰ�ں�˹̹��ţ���������}ˮϡጵĴ�������VƤ��̎����Ч��һ��������
�ڌ��3�У��c���y(t��ng)��ÿ��2�ι�4���IMע���������^�������(y��ng)��20mg/ml�����|(zh��)�ᣨ100% SRF��ϡጴ����ݼ���V��δ�IMע���Ч��Ҳ�dz���Ч��������ڸ��yԇ���Ŀ��������ɽM�g�]���@���IJ��������c��ǰ�īI(xi��n)�Ј����ÿ��2��̎�������Ŀ���ֲ��̥��(sh��)���������䔵(sh��)���ܸ����ֵ��ע�������̎��������������FSH����(y��ng)�����ݣ�ֱ����3-5mm����(sh��)���ڃɽM�g�]�в�����ϣ����սM�Ĕ�(sh��)��߀ռ��(y��u)���������⣬�ɽM�g�����є�(sh��)��LH̎�������ѵĕr�g�g���϶��]�в����ɽM�g�o����������L�����@ʾ�ˆδ�IMע���������V�ɞ����ݵ����L�������A���ṩ�����FSH��
���3��һ�������|(zh��)��ϡጴ����ݼ���V��δ�ע���T�l(f��)��ţ���ŷ���(y��ng)���ஔ(d��ng)��(y��n)֔(j��n)?sh��)Ĝyԇ��������ڂ��y(t��ng)��ÿ��2�ε�IMע��ģʽ�����˜yԇ���H�C���������L������������ڜyԇ�ĸ�׃���g�������������������̥�a(ch��n)������Ҫ�Ŀ���ֲ��̥��(sh��)���]�в�������M�܆δ�IMע��̎���е���Ѵ�������V�Ą����]�б��yԇ����������@�cÿ��2��ע��Ą����������Ҳ����ǰ����Ćδδ�������SCע��Ą��������
5. �Y(ji��)Փ
���ĸ������������ڂ��y(t��ng)��ÿ��2�ε�IMע��̎�������������20mg/ml�����|(zh��)��ϡጵĴ�������V�δ�ע���ļt����˹���w��ţ�ij��ŷ���(y��ng)Ҳ���^�õ��������ڻ�ϴ������غ����|(zh��)��ķ������ǿ��е�����������ڰ���˹ţ��ʹ�õ��@һ�����Ƿ��(y��u)߀��̫�������������V�Ćδμ����(n��i)ע�䌢�p�ٳ���̎���еĄڄӏ��Ⱥ�̎����������e�nj����y���M(j��n)�г���̎�������Ą�����ԣ��˷����������m�������� |
